OBJETIVOS: Obtener la expresión matemática de una de las leyes de los gases ideales.
MATERIALES:
- Tubo de Schlenk
- Caperuza con conexión al sensor de presión
- Sensor de presión
- Sensor de temperatura
- LoggerPro o interfaz al PC
- Molde de bizcocho
- Placa calefactora con agitador magnético
SEGURIDAD:
- Usa gafas de seguridad.
- La placa calefactora puede calentarse mucho. Ten cuidado para evitar quemaduras.
PROCEDIMIENTO:
- Engrasa las conexiones del tubo de Schlenlk. Coloca la llave en posición cerrada y pon la caperuza al tubo.
- Conecta el sensor de presión al tubo de Schlenk.
- Conecta ambos sensores al LoggerPro o al PC.
- Llena con agua el molde e introduce en posición horizontal el tubo de Schlenk.
- Introduce el sensor de temperatura en el agua.
- Conecta la agitación magnética.
- Comienza a adquirir datos a razón de un dato cada 5 segundos durante unos 10 minutos.
- Enciende la calefacción, controlando que la temperatura no suba demasiado rápidamente. Si la temperatura llega a unos 80 ºC, apaga la calefacción y detén el experimento.
- Una vez acabado el experimento, desmonta los elementos del tubo de Schlenk, eliminando los restos de vaselina con papel de filtro.
TAREAS:
- A partir de los datos obtenidos, extrae no menos de 8 pares de datos presión-temperatura, y preséntalos en una tabla.
- Averigua qué relación hay entre las variables que se han medido y qué ley es la que se ha comprobado. ¡BIBLIOGRAFÍA!
- Realiza la(s) representación(es) gráfica(s) pertinentes según lo investigado.
- Explica qué significan los resultados obtenidos, y escribe cuál es la conclusión a la que habéis llegado, incluyendo si es posible datos de la bibliografía.
- Evalúa el procedimiento en cuanto a precisión y exactitud de los resultados. Expón detallamente debilidades y fuentes de error del método y soluciones para las mismas.
RESULTADOS:
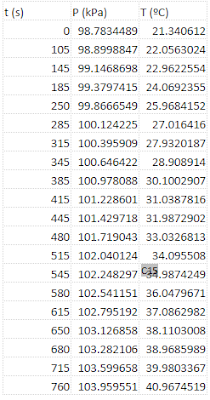
Relación temperatura-presión
CONCLUSIÓN:
En conclusión podemos observar que, según la ley de Gay-Lussac, si el volumen es constante, a mayor temperatura, mayor presión, y viceversa, ya que el cociente entre la presión y la temperatura es la constante.
EVALUACIÓN:


C=7/8=8.8
ResponderEliminar